环形RNA是一类共价闭合的单链RNA,相比线性RNA更稳定、免疫原性更低,具备特殊的空间构象。体外工程化环形RNA (in vitro circularized RNAs, ivcRNAs),正在发展为极具潜力的新型RNA药物平台。近年来研究主要围绕两大方向:一是开发为RNA适配体,用于调控靶蛋白;二是用作蛋白质翻译载体,实现长效蛋白表达。作为表达载体,工程化环形RNA的翻译通常依赖病毒来源的内部核糖体进入位点(internal ribosome entry site, IRES)启动,但是在工程化环形RNA中IRES结构是否受编码序列(cargo)影响未知。
2026年2月26日,复旦大学生物医学研究院/复旦大学附属儿科医院杨力研究组与中国科学院分子细胞科学卓越创新中心陈玲玲研究组合作,在Cell Research期刊发表题为IRES–cargo interplay structurally modulates circular RNA translation的研究论文(Letter)。该研究首次从结构层面揭示,在工程化环形RNA中,IRES序列与其驱动的cargo序列之间的相互作用会显著影响IRES结构的完整性,进而调控工程化环形RNA的翻译效率。研究提出,IRES-cargo的相互作用是评估工程化环形RNA翻译能力的重要指标,为理性设计高效翻译性能的环形RNA分子奠定理论与结构基础。

研究人员基于高效的自剪接成环系统,构建了携带不同病毒来源IRES和相同荧光素酶报告基因(firefly luciferase)的ivcRNAs。通过筛选45种IRES元件,发现第V类IRES(如Salivirus A IRES, SV-A)在多种细胞系中普遍表现出更高翻译活性。然而,SV-A驱动不同编码序列(cargo,如mCherry、水痘-带状疱疹病毒截短包膜糖蛋白E (gE) 等)时,翻译效率存在显著差异。即使经过密码子优化,某些cargo序列(如gE_jcat)在环形RNA中仍难以翻译,但在线性mRNA中却能高效翻译,提示环形构象可能改变SV-A的结构。
为进一步探究机制,团队利用in-cell circSHAPE-MaP技术,在活细胞中直接解析长链环形RNA的二级结构。结构模型显示,在高翻译活性的ivc-SV-A-mCherry和ivc-SV-A-gE_pre中,SV-A形成完整二级结构,包括关键的十字形结构域IV;而在翻译受阻的ivc-SV-A-gE_jcat中,该结构域与gE_jcat序列发生广泛碱基配对,导致十字形结构被破坏。
为验证IRES与cargo之间不利的相互作用会损害IRES结构并抑制翻译,研究者在cargo区或IRES结构域IV引入点突变,构建不同突变类型的ivcRNAs。circSHAPE-MaP分析证实,突变成功阻断了IRES与cargo间的碱基配对,恢复了SV-A结构域IV的十字形构象。进一步通过定量指标(IRES crosstalk ratio和IRES structure consistency)量化SV-A结构变化。重要的是,修复SV-A结构后,gE蛋白表达可完全或部分恢复,且表达水平与IRES结构域IV的结构完整性呈强正相关。
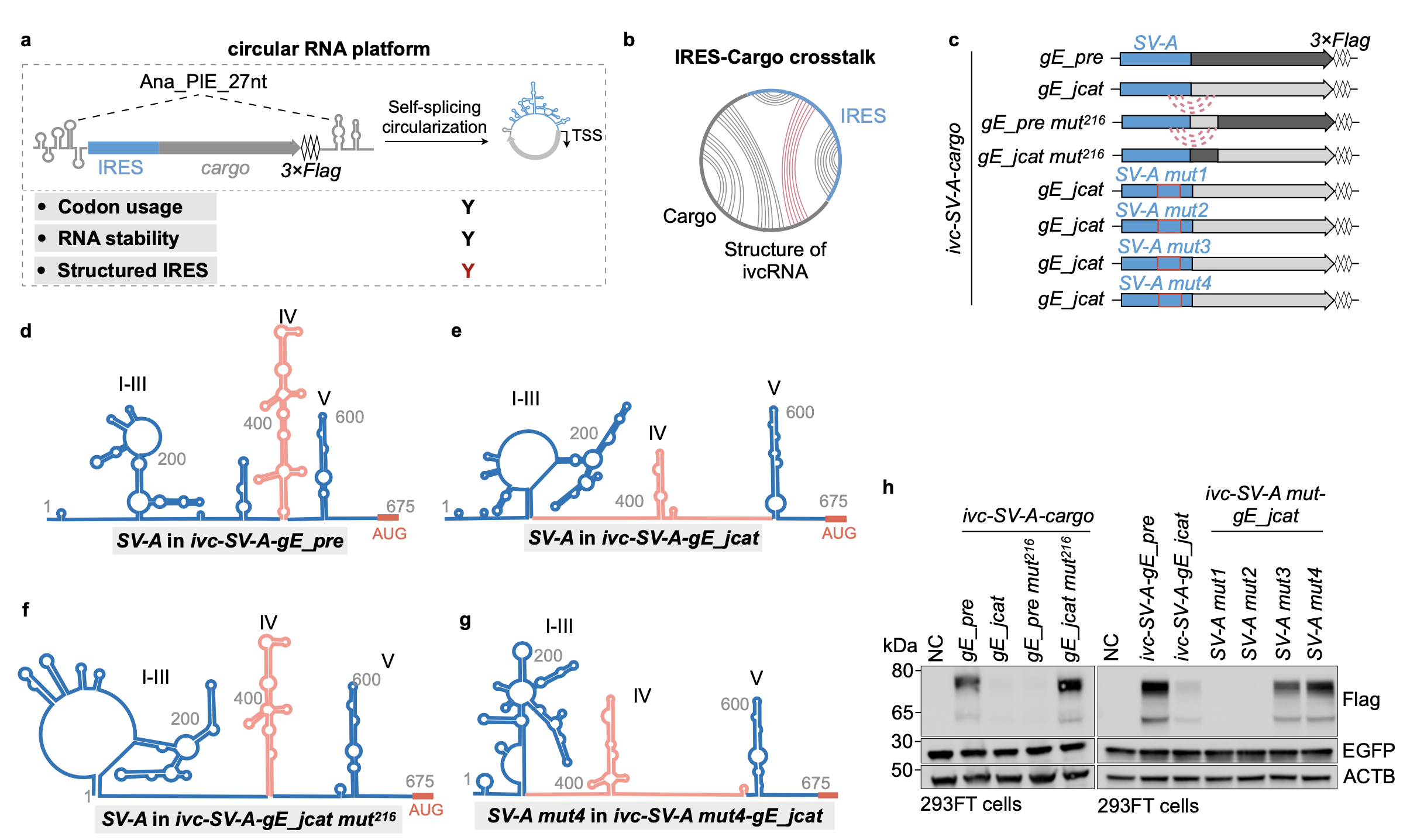
图. IRES-cargo的相互作用破坏IRES结构完整性,进而抑制ivcRNA蛋白表达,解开IRES-cargo之间的不利配对后恢复SV-A的高效翻译能力
综上,这项研究发现,在环形RNA中,IRES元件的结构折叠并非独立存在,而是受到其驱动的cargo序列的显著影响。尤其是当IRES与cargo之间发生不利的相互作用时,IRES的关键结构域会被破坏,从而翻译活性被抑制,导致蛋白质产量降低。因此,未来在环形RNA的理性设计中,除了关注IRES本身的翻译效率和cargo序列的密码子优化外,必须将IRES-cargo相互作用作为关键设计参数加以考量,通过避免或解除IRES与cargo之间的不利配对,确保IRES结构的完整性,从而实现高效、稳定的蛋白质表达,推动环形RNA疗法的临床转化。
中国科学院分子细胞科学卓越创新中心副研究员黄友葵、复旦大学生物医学研究院博士研究生陈尧琦、中国科学院分子细胞科学卓越创新中心博士研究生娄思雨、中国科学院大学杭州高等研究院博士后郜祥为论文共同第一作者,陈玲玲研究员和杨力研究员为论文共同通讯作者。该项工作获得科技部、中国科学院、上海市科委、上海市尚思科学研究院以及新基石科学基金会的经费支持。
原文链接:https://www.nature.com/articles/s41422-026-01233-9