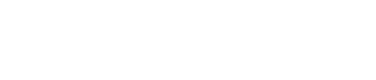乳腺癌是全球女性发病率最高的恶性肿瘤,其异质性强、转移机制复杂等特点,一直是肿瘤精准医学研究领域的热点。3月16日上午,复旦大学附属肿瘤医院放射治疗中心郭小毛、俞晓立领衔临床专家,与肿瘤研究所陈飞、沈敏洪组成跨学科研究团队,在国际期刊Cell Stem Cell上发表题为Paired patient-derived organoids reveal transcription factor-driven epigenetic remodeling in breast cancer metastasis的研究论文。该研究在全国首次构建乳腺癌类器官多组学图谱,解析乳腺癌进展过程中四种表观遗传状态,揭示驱动乳腺癌淋巴结转移的关键分子机制,突破传统乳腺癌分型局限,为乳腺癌精准治疗提供新的理论依据和实验平台。
源于临床问题,搭建类器官活体生物库
“目前广泛使用的乳腺癌分型体系,主要反映肿瘤静态分子特征,难以解释同一分型患者的不同治疗反应、临床结局等方面的差异,也无法精准还原肿瘤进展、转移的动态调控规律。”肿瘤医院放射治疗中心主任医师、教授,上海市质子重离子医院(肿瘤医院质子重离子中心)临床技术委员会主任郭小毛指出,为进一步推进乳腺癌精准治疗,这一临床问题亟需通过组建跨学科团队,来开展基础临床研究。
2021年起,研究团队着力优化乳腺癌患者来源类器官培养与体系流程,针对乳腺癌原发灶、淋巴结转移灶及癌旁正常组织的生物学特性设计定制化培养基,成功搭建高保真的配对类器官活体生物库。
据悉,肿瘤PDOs保留了原始肿瘤实性、囊性及葡萄状等异质性形态,正常乳腺组织PDOs则表现出更均一的形态特征。HE染色和免疫组化结果进一步表明,PDOs在组织学结构及ER、PR、HER2、Ki-67等关键临床标志物表达方面与来源组织高度一致,能够较好保留乳腺癌的核心分子和组织学特征,是研究肿瘤进展和转移的重要模型。
肿瘤医院放射治疗中心教授俞晓立说:“经过多维度验证,该生物库还能高度保留原始肿瘤的组织病理、分子标志物表达等核心特征,精准还原乳腺癌发生、进展与转移的动态分子变化,构建了覆盖乳腺癌发生、进展与转移过程的多组学功能模型资源库。”
创新分型维度,识别四类表观遗传状态
研究团队整合基因组、转录组、染色质可及性等多组学数据开展深度分析,首次在乳腺癌PDOs识别出四种独立于传统分型的乳腺癌表观遗传状态,第一类为基底样主导状态、第二类为静息luminal样状态、第三类为高增殖luminal-HER2相关状态、第四类为淋巴结转移相关状态。
研究团队成员、肿瘤医院肿瘤研究所教授陈飞说:“这四种状态具有明显不同的调控元件开放模式和转录程序,提示乳腺癌在表观遗传层面存在独立于传统分类的状态维度。”
“我们为进一步验证这一表观遗传状态框架的稳健性,还将PDOs中提取出的状态特异基因特征应用于多个独立乳腺癌患者队列。”研究团队成员、肿瘤研究所教授沈敏洪指出,前三种主要来源于原发灶的表观遗传状态在外部人群中均可被稳定识别,其对应的通路特征也得到重复验证,提示这一状态框架具有较好的可重复、可推广。
“研究发现的四类乳腺癌表观遗传状态,具有独特的调控模式和生物学特征,且与患者临床预后密切相关。”俞晓立说。研究后进一步发现,第二类的静息luminal样状态的患者预后最好;第一类的基底样主导状态和第三类高增殖luminal-HER2的患者,则有更高的复发风险。其中第一类的基底样主导状态还和不佳的总生存有相关性。
筛选治疗药物,基于新分型制定治疗新策略
“研究团队所识别的四类表观遗传状态,不仅能够反映乳腺癌内部更深层次的生物学差异,也具有明确的预后意义,为后续我们进一步推进精准治疗,提供了新的认知维度和科学分型。”郭小毛强调。
依托四类表观遗传状态的新分型,研究团队着手开始筛选对应的治疗药物或治疗新策略。为评估该表观遗传聚类体系的治疗指导意义,研究团队进一步对预后稍差的第一类基底样主导状态和第三类高增殖 luminal-HER2来源的PDOs进行了24种临床常用乳腺癌药物的高通量筛选,结果显示,不同表观遗传状态对应不同治疗脆弱性。其中,第三类高增殖luminal-HER2的患者对内分泌治疗、HER2靶向治疗及部分CDK4/6抑制剂表现出更高敏感性。研究团队通过进一步分层分析后显示,在ER阳性样本中,高增殖luminal-HER2的患者相较基底样主导状态的患者,对内分泌治疗反应更好。
上述结果提示,表观遗传状态框架不仅有助于刻画乳腺癌的生物学异质性,也有望为精准治疗提供新的分层依据。
锁定转移靶点,揭示驱动转移关键分子机制
肿瘤转移最可怕的地方,从来不是肿瘤走得有多远,而是它在离开之前,早已变成了另一个“自己”。因此,研究团队在研究中重点聚焦淋巴结转移相关表观遗传状态,并通过整合多组学数据构建转录因子—靶基因调控网络,筛选出MEF2A、TFAP4、BHLHA15等驱动该状态的核心转录因子,其中TFAP4与BHLHA15的协同调控作用最为显著。
后经细胞与动物实验证实,敲除TFAP4或BHLHA15后,癌细胞的上皮间质转化、细胞黏附等转移相关能力明显减弱,移植瘤的肺、肝转移病灶也显著减少,该结果在多种乳腺癌模型中均得到验证。“这表明,乳腺癌淋巴结转移并非单纯的细胞表型变化,而是由一套稳定且可干预的表观遗传调控网络驱动,TFAP4、BHLHA15等转录因子,有望成为阻断乳腺癌转移的潜在治疗靶点。”陈飞解释。
俞晓立最后介绍了本次研究成果的多个创新点:“首先通过建立乳腺癌PDO生物库并开展系统性多组学分析,在全球描绘了首张乳腺癌进展过程中的表观遗传变化图谱,提出了四种具有不同生物学特征的表观遗传状态。本项研究成果不仅深化了对乳腺癌异质性和转移机制的认识,也为乳腺癌患者分层和精准治疗提供了新的思路。”
郭小毛表示,“未来将进一步依托PDO模型,探索建立新辅助放疗分层体系并解析局部晚期乳腺癌放疗抵抗的分子机制,为乳腺癌患者精准治疗策略的优化提供新的研究基础。”