软脑膜转移是肺癌、乳腺癌等实体瘤最致命的中枢神经系统并发症——肿瘤细胞一旦侵入脑脊液,患者自然生存期仅约两个月,且伴随剧烈头痛、认知衰退等严重症状。临床治疗始终面临一个根本困境:在转移发生的极早期,肿瘤细胞如何远程“改造”中枢屏障,为后续入侵铺平道路?这一认知盲区,导致早期预警与干预手段长期缺失。
复旦大学脑科学转化研究院研究员迟喻丹长期聚焦中枢神经系统屏障系统研究。该团队2026年4月3日发表于Nature Cancer的最新研究“Leptomeningeal metastatic cancer cells induce a permissive choroid plexus vasculature through extracellular-vesicle-derived 5-HIAA signaling”将视角聚焦于中枢边界的另一道关键防线——脉络丛血管屏障,深入揭示了肿瘤细胞在抵达中枢之前,如何远程“异化”这一结构,为自身入侵铺平道路。外周肿瘤细胞通过细胞外囊泡递送代谢分子5-HIAA,精准靶向脉络丛血管内皮细胞,提前瓦解中枢边界的防御体系,待“防线崩溃”后再从容定植。
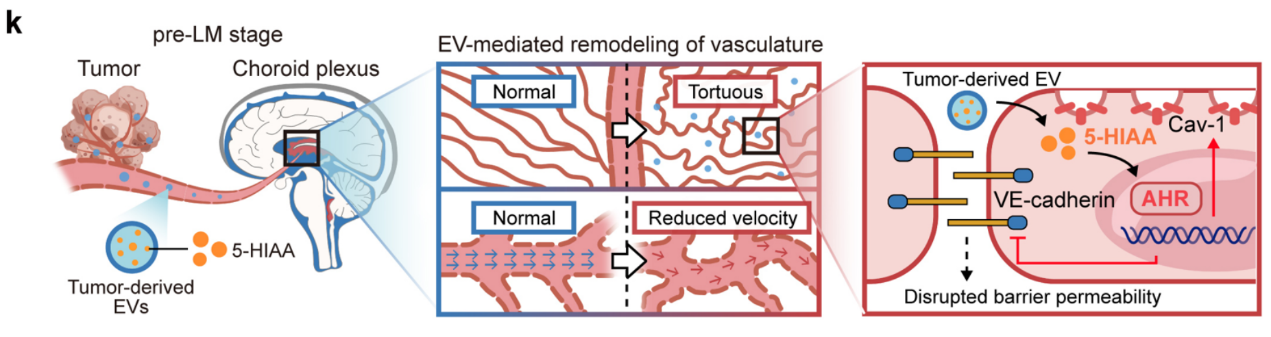
脉络丛是血—脑脊液屏障的核心结构,也是肿瘤细胞进入软脑膜间隙的关键门户。研究团队通过构建软脑膜转移小鼠模型,精准定义了疾病进展的关键窗口期。基于这一模型,团队联合脑脊液非靶向代谢组学与MALDI-MSI空间代谢组学技术,发现:即使在癌细胞尚未到达中枢的阶段,脉络丛已发生全面的代谢重编程,氨基酸代谢与脂质代谢两大核心通路显著重塑。更为关键的是,脉络丛的血管结构与功能发生了全面“异化”:血管形态呈现异常迂曲的“肿瘤样”改变,伴随血流动力学紊乱与血管屏障完整性破坏。这种病理改变具有高度的脉络丛组织特异性,在机体其他血管屏障结构中并未出现——这意味着,肿瘤细胞在“抵达战场”之前,已经远程改写了中枢边界的“地形图”。

通过对脑脊液与脑组织差异代谢物的交叉验证,团队锁定了5-羟吲哚乙酸(5-HIAA)为核心功能分子。该分子在转移前阶段的脑脊液与脉络丛中特异性显著升高,并在软脑膜转移患者样本中得到验证。脉络丛中升高的5-HIAA并非来自中枢局部合成,而是直接来源于外周原发肿瘤细胞。肿瘤细胞通过分泌携带大量5-HIAA的细胞外囊泡(EVs),经血液循环靶向递送至脉络丛血管内皮细胞。5-HIAA进入血管内皮细胞后直接激活AHR通路,破坏血管屏障的核心结构,最终造成脉络丛血管内皮屏障完整性丧失,为癌细胞穿越血管屏障、完成中枢定植创造条件。
本次研究的突破在于:将“转移前微环境”的经典理论拓展至中枢神经系统软脑膜转移范畴,揭示了肿瘤细胞通过细胞外囊泡递送代谢分子、远程靶向调控中枢边界血管屏障的全新模式。这一发现不仅揭示了脑膜转移瘤独特的致病规律,更提示我们:要真正拦截这类肿瘤,战场不应局限在中枢内部,而应前移至肿瘤细胞尚未抵达的“转移前阶段”。