4月1日,《肝脏病学杂志》(Journal of Hepatology)在线发表了复旦大学放射医学研究所畅磊研究员、邵春林研究员与南方科技大学陈曦教授团队的合作研究成果,题为“Chromatin remodeling in pericentral hepatocytes modulates MASH through CYP450 activity”。该研究系统揭示了位于肝小叶中央静脉周围的 Lgr5⁺肝细胞中,染色质重塑因子DPF2通过调控 CYP450代谢酶活性与全反式维甲酸(atRA)平衡,进而影响放射性肝损伤、代谢相关脂肪性肝炎(MASLD)发生发展的全新机制,为 放射性肝损伤、MASLD/MASH的发病机理研究与临床干预提供了重要理论依据。

富含亮氨酸重复序列 G蛋白偶联受体5(Lgr5)通常作为活跃自我更新组织的干细胞标志物,其在肝脏中的功能长期存在争议。早期研究曾认为Lgr5⁺肝细胞具有肝干细胞特性,后续研究则逐步修正了这一观点,证实这类细胞在肝脏稳态维持与组织再生中作用有限,主要用于维持自身谱系,但其具体生理功能与病理意义仍未被充分阐明。肝脏以小叶为基本功能单位,沿门静脉至中央静脉呈现显著的代谢分区,其中中央静脉周围Lgr5⁺肝细胞虽仅占肝脏细胞总数的 3%–5%,却参与营养代谢与肝脏疾病进程,而这类少量细胞如何调控整体肝脏代谢状态,一直是领域内尚未解答的关键科学问题。
在本项研究中,团队综合运用基因工程小鼠模型、单细胞转录组、空间转录组、染色质可及性分析(ATAC-seq)以及表观遗传修饰检测(CUT&RUN、CUT&Tag)等技术,系统解析了 Lgr5⁺肝细胞中SWI/SNF染色质重塑复合物关键亚基DPF2的功能。研究发现,Lgr5⁺肝细胞中DPF2的缺失会显著提高CYP2家族代谢酶基因启动子区域的染色质可及性与激活型表观修饰,进而增强CYP2对全反式维甲酸(atRA)的分解代谢。肝脏内atRA水平下降会导致AMPK磷酸化水平降低,无法有效维持脂质代谢稳态,最终显著加剧饮食诱导的肝脏脂质沉积、炎症及脂肪性肝炎病变。同时,该研究还观察到,Lgr5⁺肝细胞DPF2敲除小鼠同样表现出明显的放射性肝损伤表型,提示这一机制在辐射损伤与代谢肝病中具有共通的重要意义。这一发现也为肝病研究提供了重要方法学启示,提示传统批量组学或全肝基因操作可能掩盖空间限制性细胞群体驱动疾病的关键机制。
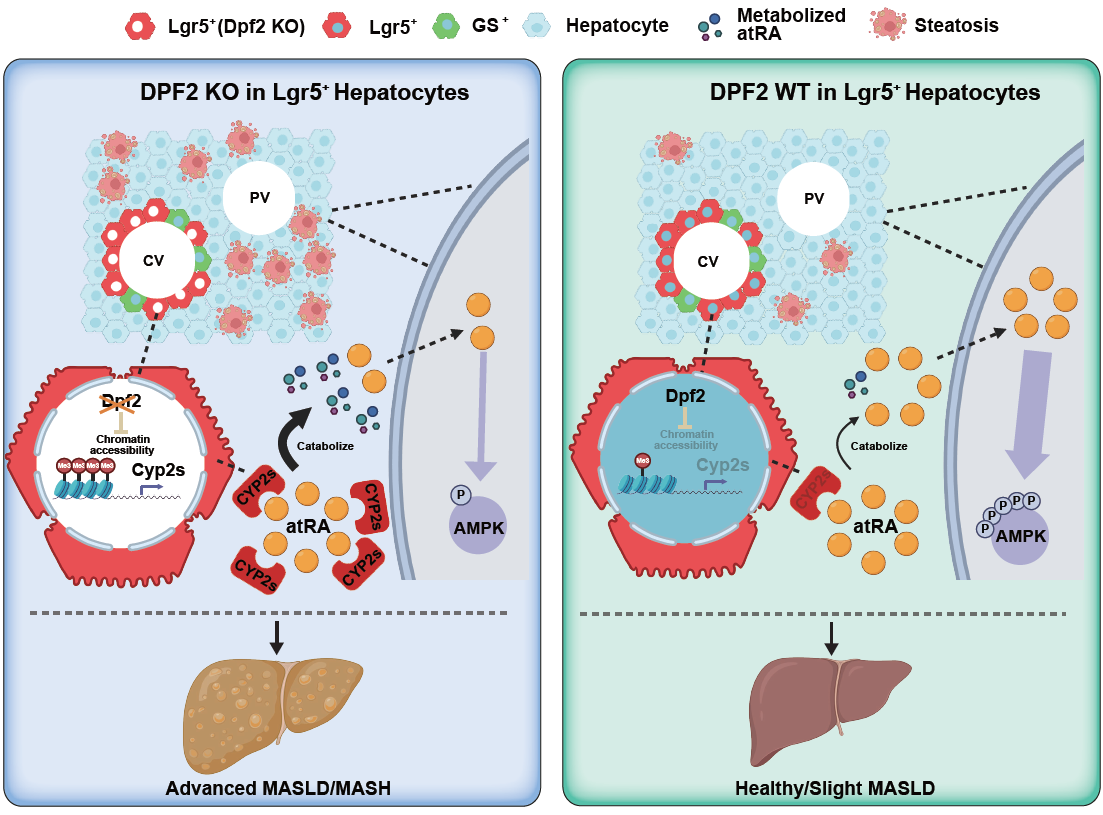
该成果不仅深化了对 Lgr5⁺肝细胞功能的认知,也为放射性肝损伤、代谢相关脂肪性肝病的防治提供了atRA补充、CYP2酶抑制及AMPK激活等潜在干预策略。研究工作主要由张志森博士生、卢双双硕士、舒银银博士后等同学完成。
全文链接:https://www.journal-of-hepatology.eu/article/S0168-8278(26)00190-X/fulltext