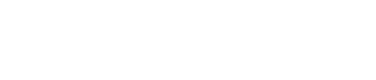近日,Protein & Cell发表了黄荷凤院士团队的最新研究成果:“Biallelic variants in RBM42 cause a multisystem disorder with neurological, facial, cardiac, and musculoskeletal involvement(RBM42双等位基因变异导致神经、面容、心脏和肌肉骨骼的多系统异常)”(原文链接:https://pubmed.ncbi.nlm.nih.gov/37294900/)。本研究基于临床获得的罕见病例,通过家系全外显子组测序,发现RBM42可能是常染色体隐性遗传神经发育障碍综合征的新致病基因。在此基础上,利用细胞、真菌和小鼠模型,研究基因型与表型的相关性。本研究首次将RBM42基因与人类具体疾病相关联,为进一步了解RNA结合基序蛋白的生物学意义奠定基础,并为相关疾病诊断和治疗提供理论依据。
神经发育障碍 (neurodevelopmental disorders, NDDs) 是一种常见的出生缺陷,表现为大脑发育或功能受损,影响认知、语言、情感和运动等正常发育,全球有超过3%的儿童受累。常见的NDDs包括智力障碍、注意力缺陷/多动症、自闭症谱系障碍和癫痫等。大部分NDDs 是综合征性疾病,除神经系统症状外,还累及其它系统,尚缺乏有效的治疗手段,严重影响患者的生存和生活质量,给家庭和社会造成巨大负担。早期的筛查和诊断对NDDs 的预防控制有重要的科学价值和社会意义。高通量测序技术可以检测到基因组中绝大多数重要变异,也为NDDs 的分子诊断和寻找新的致病基因提供了有效的方法。然而,NDDs 具有高度的遗传异质性,目前仍有超过一半的NDDs 患者未找到明确的遗传学病因。
本课题组长期致力于出生缺陷相关的遗传学诊断及机制研究工作。前期工作中,我们通过全外显子组测序,在以中枢神经系统异常、特殊面容、先天性心脏病、严重发育迟缓等异常为特征的罕见病例中发现RBM42 可能是一个新的常染色体隐性遗传神经发育障碍综合征的致病基因。
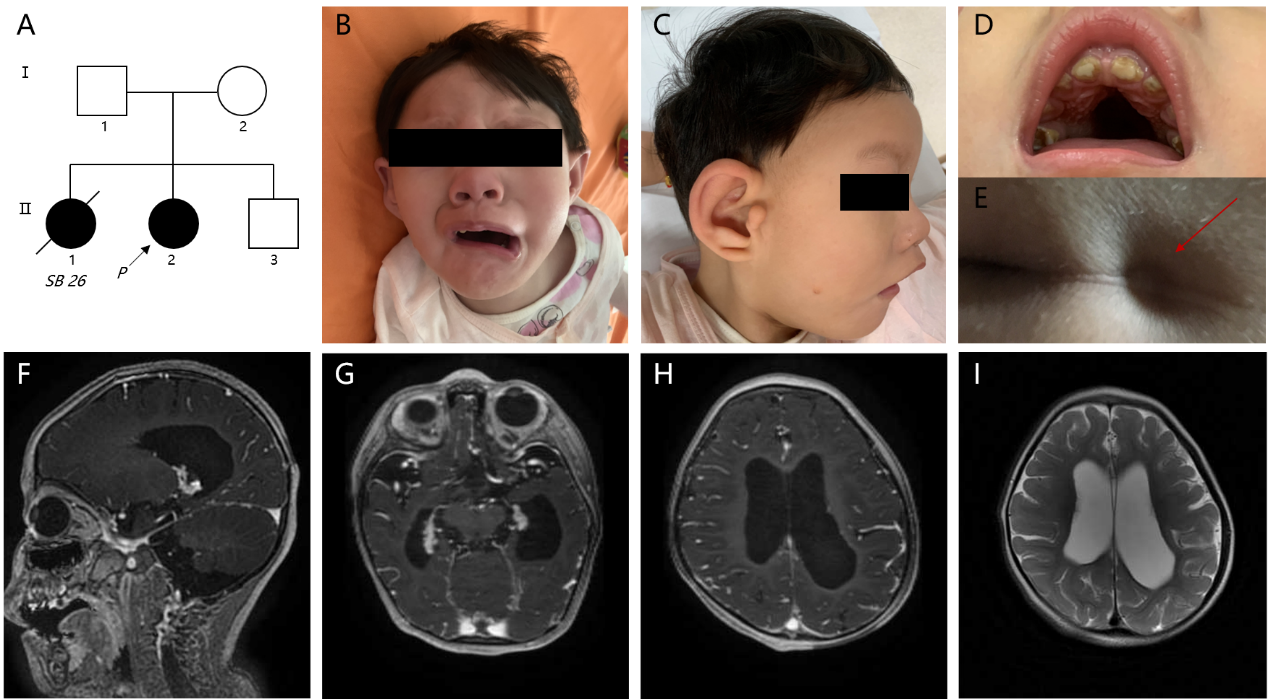
图1 先证者的临床表现
经过对先证者进行染色体核型分析、染色体微阵列检测和线粒体测序,结果均为阴性。行家系全外显子组检测时,在已经的致病基因里亦未发现可疑的致病位点,但数据再分析时发现先证者存在高度可疑致病变异:NM_024321.5(RBM42):c.[304C>T];[1312G>A], p.[(Arg102*)];[(Ala438Thr)]。RBM42基因编码RNA 结合基序蛋白42,是一个重要的剪接调控因子,在人体中广泛表达。目前,对RBM42 基因的研究尚少,其参与疾病的作用机制尚不明确。但是,已有研究表明RBM42与引起Au-Kline 综合征的HNRNPK 基因关系密切。
HNRNPK基因致病性变异引起的Au-Kline 综合征以常染色体显性方式遗传,主要表现为全面发育迟缓,张力减退,智力障碍,存在可变的自主神经功能障碍,大多数患者存在先天性心脏病,灰质异位,胼胝体发育不全等。典型的面部特征包括长睑裂,上睑下垂,浅眼眶,耳突出,耳廓异常,宽鼻翼,舌中线深和下垂嘴。其它异常包括颅缝早闭,喂养困难,视力问题,听力障碍,肾积水,腭异常,少牙等。多学科会诊认为RBM42 突变患者表型与Au-Kline综合征高度重叠,可归为Au-Kline综合征的一种亚型。
本研究首先建立了患者家系的LCLs细胞系,发现先证者的RBM42 mRNA和蛋白表达水平均比其父母低。293T的过表达实验证实,R102*突变导致了无义介导的RNA降解,无最终蛋白产物,A438T突变的表达量也比野生型低。Co-IP实验进一步证实A438T突变影响了RBM42与HNRNPK的结合。免疫荧光结果说明,突变虽然影响了RBM42的表达,但未改变其与HNRNPK在细胞内的定位。(图2)

图2 野生型和突变型RBM42在不同细胞系中的表达情况
之前已有研究表明,人类RBM42是引起小麦赤霉病的禾谷镰刀菌中pre-mRNA 剪接调节因子FgRbp1 的直系同源物,能够完全弥补ΔFgRbp1引起的生长缺陷。因此,在此基础上,本研究构建了突变型的回补载体,转化ΔFgRbp1缺陷型禾谷镰刀菌,观察菌丝的生长情况。结果发现,ΔFgRbp1::RBM42R102*菌株生长情况与ΔFgRbp1菌株相似,约40%的ΔFgRbp1::RBM42A438T菌株能回复到与野生型相似的生长情况。禾谷镰刀菌的回补实验证实R102*是无效变异,A438T是亚效变异。
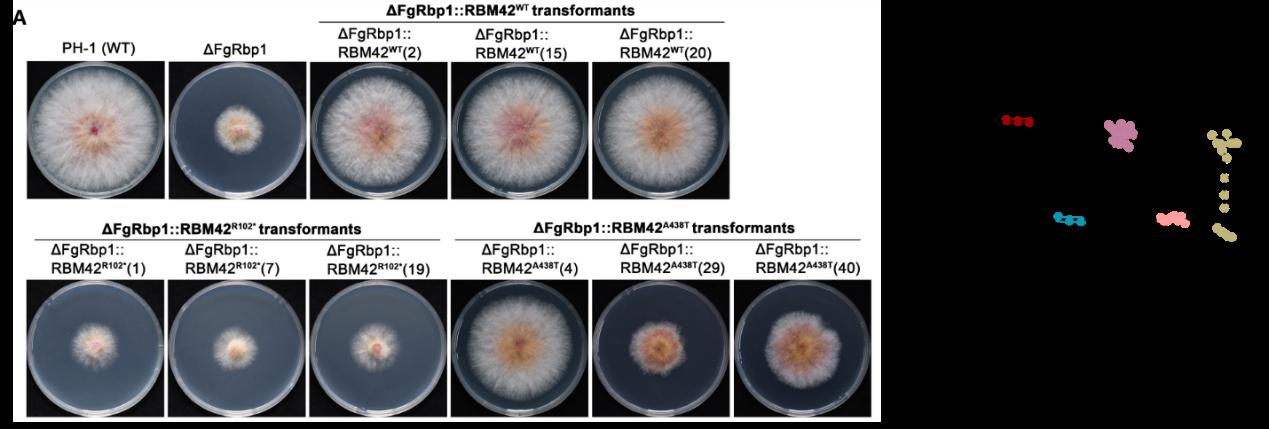
图3 禾谷镰刀菌的回补实验
本研究还利用CRISPR/Cas9技术对单倍体细胞进行基因编辑,基于单倍体精子快速获得了突变小鼠模型。双突变小鼠生长发育严重受限,且胚胎致死。进一步对E9.5的小鼠胚胎进行了RNA-seq分析,发现变异影响了小鼠神经、心脏发育相关基因的表达和剪接,与患者的主要表型相符,也应证了RBM42主要是通过影响重要的可变剪接事件,进而影响胚胎的正常发育。
图4 小鼠模型和部分RNA-seq结果
本研究初步证实RBM42是一个新的神经发育障碍综合征致病基因。临床评估、遗传分析、细胞功能实验和突变模型研究的结果支持RBM42通过影响选择性剪接,在维持胚胎发育所需的正常细胞生长方面发挥重要作用。
本论文由复旦大学附属妇产科医院黄荷凤院士、徐晨明研究员、张静澜研究员为共同通讯作者,中国福利会国际和平妇幼保健院陈毅瑶、杨秉鑫、中科院分子细胞科学卓越创新中心张晓宇、复旦大学附属妇产科医院陈松长为共同第一作者。中科院分子细胞科学卓越创新中心李劲松院士和浙江大学农业与生物技术学院马忠华教授对本研究给予大力支持。