2024年1月1日,复旦大学附属眼耳鼻喉科医院麻醉科李文献/韩园课题组在麻醉领域期刊Anesthesiology上发表了题为“Medial Septal Glutamatergic Neurons Modulate States of Consciousness during Sevoflurane Anesthesia in Mice”的最新研究成果。课题组发现,位于基底前脑隔区的内侧隔核(Medial Septum,MS)中一类兴奋型神经元——谷氨酸能神经元调控七氟烷全身麻醉。该研究受到编辑和审稿专家的好评,入选为当月推荐文章“This Month in Anesthesiology”。

全身麻醉已问世近两百年,每年全球有数亿患者接受全身麻醉,麻醉对全球健康与疾病负担具有重大的影响。虽然近年来麻醉安全得到了显著改善,但仍面临不少问题与挑战,究其根本在于全麻机制尚未阐明。正是因为如此,Science杂志在其创刊125周年之际继续将全麻药物的作用机制列为未来亟待解决的125个前沿科学问题之一。
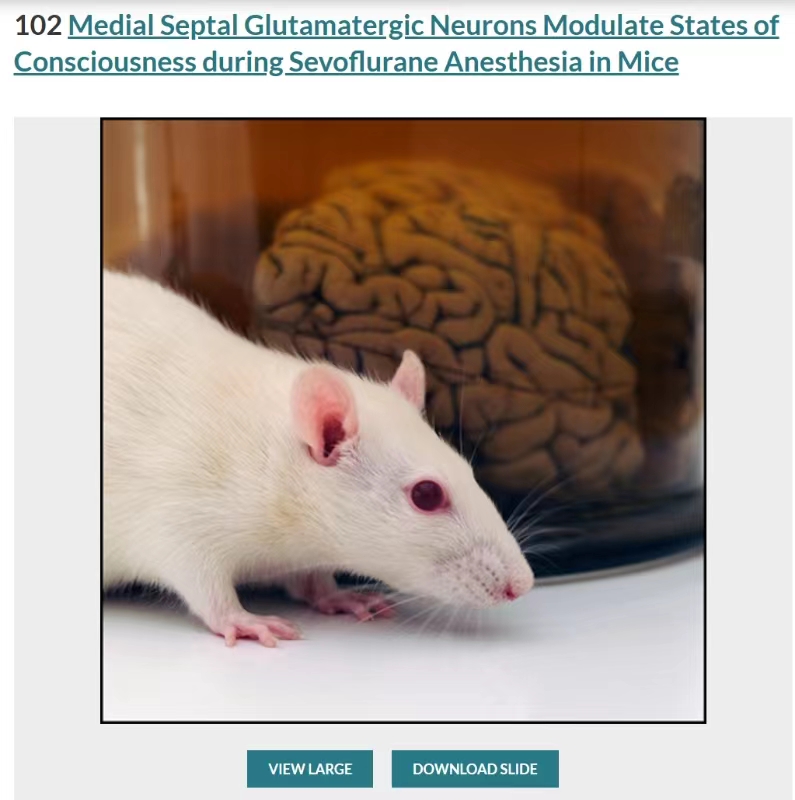
期刊编辑撰稿配图,在“This Month in Anesthesiology”板块介绍本研究
研究人员利用Vglut2-Cre小鼠,通过在体光纤钙信号和脑电肌电记录,发现内侧隔核谷氨酸能神经元群体的钙信号水平在暴露于七氟烷之后呈浓度依赖性下降,而关闭七氟烷之后,钙信号水平逐渐恢复。有意思的是,结合脑电肌电分析发现,在关闭七氟烷之后,该神经元群体的钙信号水平在苏醒早期、小鼠翻正反射恢复之前就已经显著上升,且在翻正反射恢复之后进一步增加。这提示MS谷氨酸能神经元可能促进了从麻醉到觉醒的意识状态转换,并且对麻醉苏醒后维持觉醒状态起到重要作用。

在此基础上,研究人员利用化学遗传学方法特异性操控小鼠MS谷氨酸能神经元活性。研究发现,抑制该神经元群体,小鼠对七氟烷麻醉的敏感性增高,麻醉诱导加快而苏醒延迟;而激活该神经元群体则得到相反的结果,小鼠对七氟烷麻醉的敏感性降低,麻醉诱导所需的时间更长,而苏醒增快。
光遗传学方法可以对神经元活性进行精度更强且可逆的毫秒级操控。课题组进一步使用光遗传学方法研究了激活该神经元群体在麻醉稳定维持阶段对小鼠意识状态的影响。结合脑电肌电记录和行为学分析显示,使用473纳米蓝光特异性激活处于麻醉稳定维持状态中的小鼠MS谷氨酸能神经元,能迅速诱导大脑皮层活化和行为觉醒,脑电从低频高幅的慢波活动转换为高频低幅的脑电波形,δ波比例显著下降而β波、γ波比例显著增高,实验组小鼠普遍出现了翻正反射恢复甚至可以行走。

研究人员进一步通过提高七氟烷浓度诱导小鼠出现稳定至少5分钟的脑电爆发抑制波,此时再给予蓝光刺激,结果发现,小鼠依旧出现了明显的觉醒行为,并且脑电爆发抑制率显著下降。

复旦大学附属眼耳鼻喉科医院麻醉科李文献教授为文章的通讯作者,夏俊明博士(2021级博士研究生)为第一作者,樊炳乾博士(2020级博士研究生)为共同第一作者,韩园副教授对课题给予了关键指导。研究过程中还得到复旦大学基础医学院黄志力教授、曲卫敏教授的悉心指导和帮助。
近年来围绕伏隔核调控七氟烷全身麻醉中的意识状态转换的细胞及环路投射机制,课题组在Current Biology(2021)和Anesthesia and Analgesia(2023)杂志相继发表相应重要发现。本研究是在基底前脑参与全麻意识改变机制研究上取得的又一项成果,期望该系列的研究为更好地掌控临床麻醉安全、加快术后康复,以及未来研发更理想的麻醉药物提供理论依据。
原文链接:https://pubmed.ncbi.nlm.nih.gov/37812765
DOI:10.1097/ALN.0000000000004798