腺苷受体属于G蛋白偶联受体家族,包括A1R、A2AR、A2BR和A3R四种亚型,每种亚型都有独特的药理特征和组织分布。A2AR/A2BR作为代谢型免疫检查点,其表达异常与肿瘤细胞免疫逃逸密切相关。研究表明,A2BR主要表达在髓系细胞和癌细胞上,这与主要表达在T细胞上的A2AR构成了潜在互补。因此,同时阻断A2AR/A2BR信号传导,在肿瘤免疫治疗方面有着巨大的潜力。然而目前仅有一个A2AR/A2BR双重拮抗剂Etrumadenant(AB928)处于II期临床研究阶段,并且它存在较高的A1R拮抗活性和A2AR/A2BR双靶点活性均衡性不佳的问题。因此,开发具有抗肿瘤活性的新型A2AR/A2BR双重小分子拮抗剂具有重要意义。
复旦大学药学院王永辉教授/谢琼副教授课题组的研究方向之一是新型A2AR/A2BR小分子拮抗剂的发现及其肿瘤免疫治疗研究,先后于2020年、2022年和2023年在药物化学领域期刊Journal of Medicinal Chemistry上发表一篇Miniperspective综述(J. Med. Chem. 2020, 63, 12196−12212)和两篇研究论文(J. Med. Chem. 2022, 65, 4367−4386;J. Med. Chem. 2023, 66, 4734−4754)。
3月14日,王永辉教授/谢琼副教授课题组与华东师范大学生命科学学院卢伟强研究员课题组合作,再次在Journal of Medicinal Chemistry期刊上发表研究论文“Subtle Structural Changes across the Boundary between A2AR/A2BR Dual Antagonism and A2BR Antagonism: A Novel Class of 2 Aminopyrimidine-Based Derivatives”。该论文发现了一类新型吲哚类A2AR/A2BR双靶点小分子拮抗剂和A2BR选择性小分子拮抗剂,阐明了吲哚环的结构微小变化产生A2AR/A2BR双靶点活性或A2BR单靶点活性的原因和体外抗肿瘤机制。
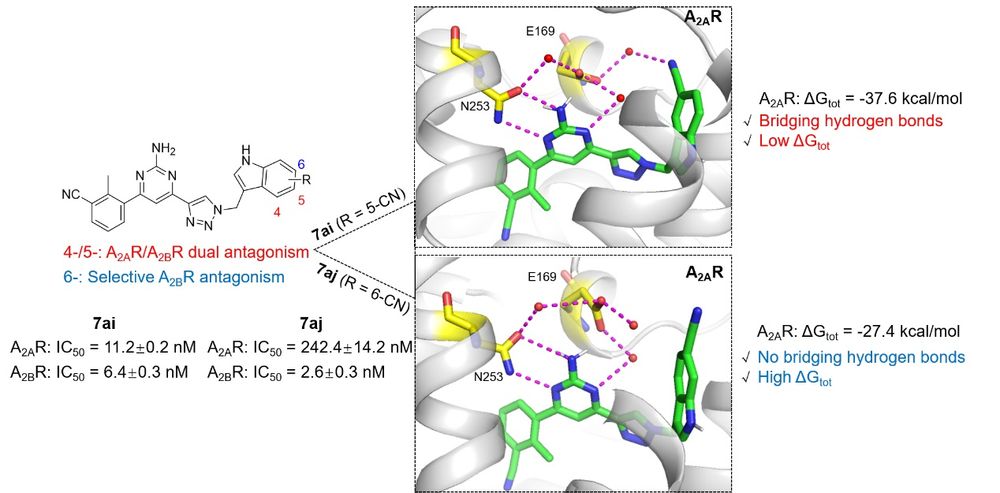
图 1. 新型吲哚类A2AR/A2BR双靶点拮抗剂7ai和A2BR选择性拮抗剂7aj的发现
本研究首先对临床试验进展最快的化合物AB928进行初步结构探索,发现了一类含有吲哚结构并具有A2AR/A2BR双靶点拮抗活性的苗头化合物,该类化合物对其他腺苷受体亚型A1R/A3R亲合性较低。随后研究发现,吲哚环的结构微调会对A2AR/A2BR活性和选择性产生显著影响(图1),在吲哚4、5位取代会产生强效的A2AR/A2BR双靶点作用,而在吲哚6位取代则会产生高选择性的A2BR拮抗作用。分子动力学模拟显示,5-氰基吲哚化合物7ai通过水分子与A2AR中的E169或F168形成稳定的桥连氢键作用,其结合自由能较低。6-氰基吲哚化合物7aj的氰基朝向不能通过水分子与周围氨基酸形成稳定氢键,导致A2AR拮抗活性明显降低。进一步的作用机制研究表明,化合物7ai通过下调免疫抑制分子PD-1和TIM-3的表达有效增强了T细胞的激活;经典的MC38-OVA/OT-I细胞毒性T淋巴细胞杀伤试验表明,化合物7ai可以增强T细胞的细胞毒性功能(图2)。这项工作优化出了比临床化合物Etrumadenant具有更高A2BR活性、更均衡A2AR/A2BR双靶点活性且几乎无A1R/A3R活性的双靶点拮抗剂7ai,以及A2BR选择性拮抗剂7aj,为后续获得新型A2AR/A2BR双靶点拮抗剂或A2BR选择性拮抗剂提供了新的先导化合物和优化策略。
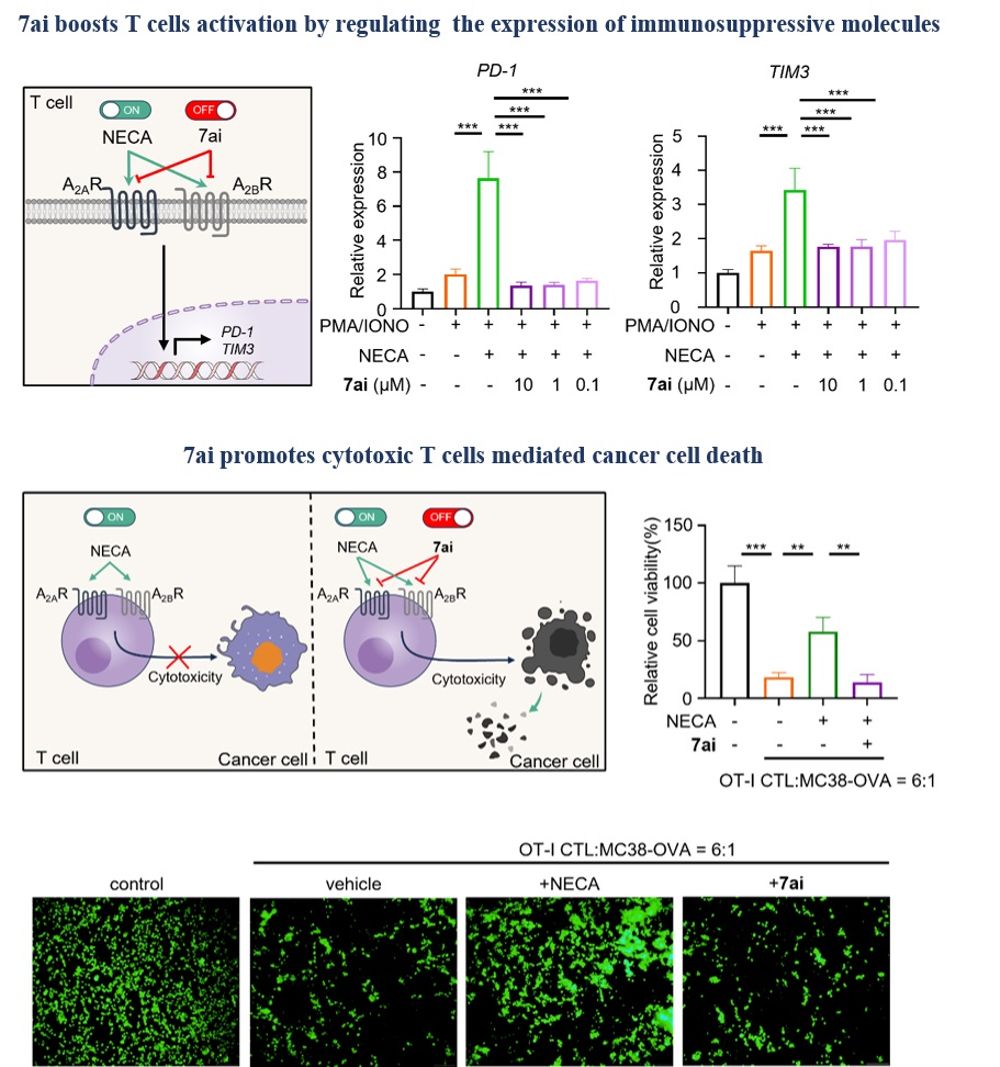
图 2. A2AR/A2BR双靶点拮抗剂7ai的体外抗肿瘤机制研究
复旦大学药学院药物化学系2020级博士生王豪杰、副研究员李嫣,华东师范大学生命科学学院2021级硕士生杨新宇为本文的共同第一作者;复旦大学药学院谢琼副教授、王永辉教授和华东师范大学卢伟强研究员为本文的共同通讯作者。
原文链接: https://doi.org/10.1021/acs.jmedchem.4c00250
王永辉教授、谢琼副教授课题组介绍
复旦大学药学院药物化学系王永辉教授、谢琼副教授课题组主要研究方向是自身免疫性疾病与肿瘤免疫治疗小分子药物的发现,以及有机与药物化学新方法新技术的研究。现有讲座教授1名,副教授2名,在读博士研究生3名、在读硕士研究生4名,已毕业博士7名、硕士5名。课题组先后承担国家科技重大专项、国家自然科学基金面上项目、上海市科委生物医药领域科技支撑项目、上海市自然科学基金及药企合作等科研项目20余项,累计经费超过1100万元。近5年在J Med Chem, Eur J Med Chem, J Org Chem, ACS Med Chem Lett等学术期刊发表通讯作者SCI论文20余篇;申请中国专利16项(已获6项授权),2项国际PCT专利申请进入美国、日本、欧洲(已获6项国际专利授权)。在自身免疫病和肿瘤免疫治疗小分子药物研究中,发现多个具有开发潜力的候选药物,正在进行临床前评价。