联合抗逆转录病毒治疗(combination antiretroviral therapy, cART)显著降低了艾滋病病毒(HIV)感染者的死亡率,HIV感染者的存活期显著延长。在欧美发达国家,HIV感染者的期望寿命从1996年的55岁增加到2005年的70岁,如今更已接近一般人群,HIV感染者群体的老龄化趋势日渐凸显。非HIV感染直接相关的慢性疾病(如心血管疾病、中枢神经系统疾病、肝肾疾病等年龄相关慢性疾病)的发病风险增加,且在HIV感染者死亡中的归因比例增加,其中以动脉粥样硬化性心血管疾病(包括心肌梗塞和卒中)最为突出。近期研究显示,卒中及多种心血管疾病在HIV感染者中发生提前,且患病率显著高于同年龄段的HIV阴性对照人群。这些提示HIV感染者的心血管疾病高风险除部分可归因于其较高吸烟率、抗病毒药物治疗引起的脂肪代谢障碍、代谢综合征等外,应还存在其他的独特的致病因素,研究证据显示,可能与HIV感染直接或间接引起的持续炎症反应和免疫激活有关。越来越多的研究发现,尽管有效的cART后体内HIV病毒载量低于检测水平,HIV感染者的免疫激活和炎症生物标志物虽较治疗前降低,但仍高于HIV阴性对照人群。
近日,复旦大学公共卫生学院何纳教授团队的研究提示,应该加强对HIV感染者心血管疾病相关指标的筛查。10月18日,研究成果以《基于CHART队列基线横断面评估的HIV感染与颈动脉内膜中层厚度之间的年龄别关联》为题在线发表于《柳叶刀-艾滋病》(The Lancet HIV)。
该研究致力于比较HIV感染者和年龄、性别匹配的社区HIV阴性对照人群的亚临床动脉粥样硬化指标水平,并综合考虑传统心血管病致病因素的影响。研究团队发现,尽管HIV感染者的传统心血管风险评分(Framingham Risk Score, FRS)显著低于HIV阴性对照,但是HIV感染者的亚临床动脉粥样硬化指标平均水平明显高于同年龄段的HIV阴性对照,且这种差异在年轻组表现更为显著(18–29 岁:568 vs 477µm,p <0.0001;30–44 岁:640 vs 586 µm,p<0.0001;45–59 岁:789 vs 730 µm;p=0.0002;60–75岁:915 vs938 µm;p=0.321);经多因素分析,这种差异在年轻组仍具统计学意义。这可能部分由于较高年龄组高水平的传统心血管危险因素(如高血压、高血脂等)掩盖了HIV感染的效应。研究团队还发现,部分年轻的HIV感染者已经出现亚临床动脉粥样硬化,而这在同年龄段的HIV阴性人群中一般少见。该研究表明,即使接受抗病毒治疗,HIV感染者仍然面临着高于一般人群的动脉粥样硬化风险,且一些HIV感染者在年轻时就出现亚临床动脉粥样硬化。因此,应该加强对HIV感染者心血管疾病相关指标的筛查。
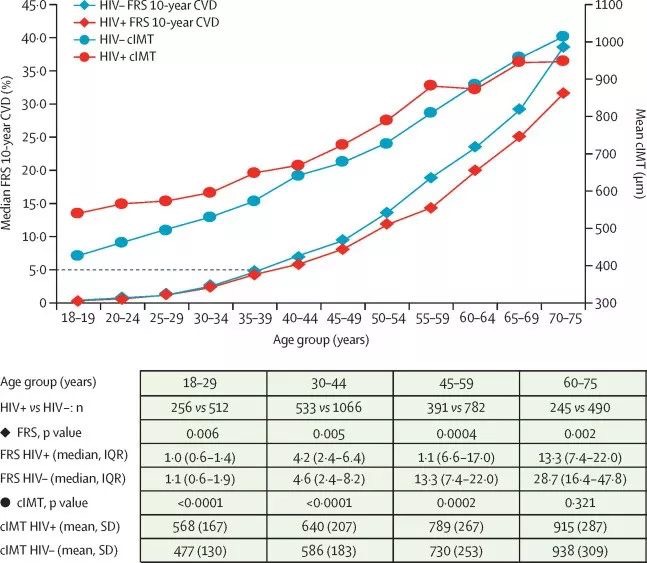
图1:不同年龄段HIV感染者和HIV阴性对照颈动脉内膜中层厚度(均数±标准差)与Framingham心血管评分(中位数,四分位数)平均水平。
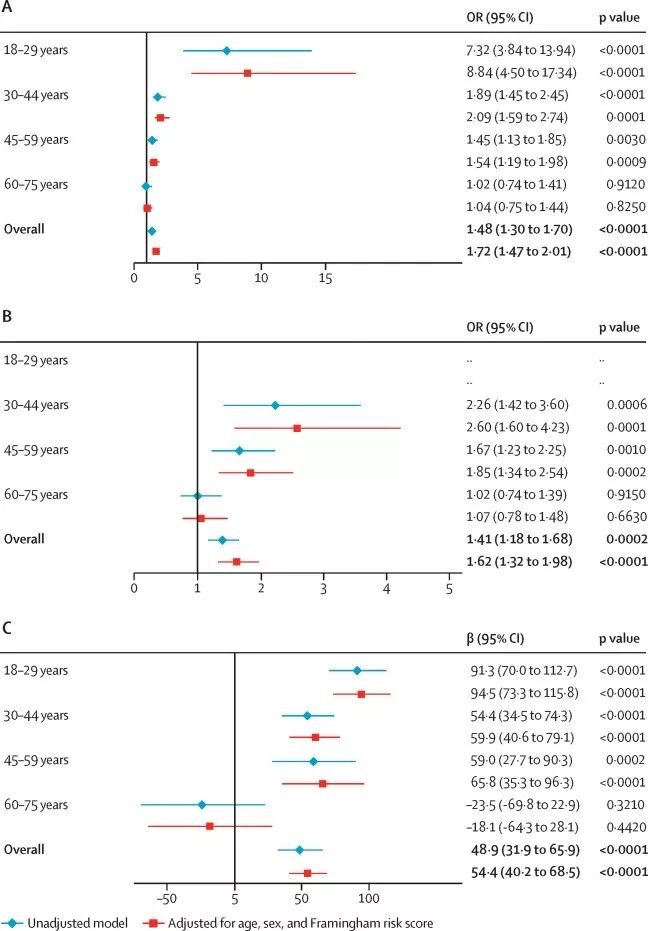
图2:HIV感染与颈动脉中层厚度年龄别关联的单因素与多因素回归模型结果。(A) cIMT ≥780 μm (B) cIMT > 1000 μm (C) cIMT连续性变量
《柳叶刀-艾滋病》同期邀请了国际艾滋病专家Esteban Martinez教授撰写了专家述评,指出“该项研究为之前研究结果的差异提供了合理的解释,并证实在调整年龄、性别及其他已知心血管危险因素后,HIV感染者即使经过抗病毒治疗,其体内HIV病毒载量得到成功抑制,但仍面临较高的动脉粥样硬化发生风险”。评论指出,该研究有两项重要的现实意义。首先,各类适用于普通人群心血管病发病风险的评分指数在应用于HIV感染人群时,会低估其亚临床动脉粥样硬化风险。其次,即使HIV感染者体内病毒复制水平获得成功抑制,也会有较高的亚临床动脉粥样硬化风险;而一旦出现动脉粥样硬化病,他们可能需要目前艾滋病临床治疗指南中未被提及的、而被推荐于治疗普通人群中同类疾病的其他治疗选项。